近日,公司张媛教授、李星教授和闫亚平教授团队联合在Neuron上发表一项突破性研究成果,揭示了少突胶质细胞独特的糖酵解代谢偏好及其通过蛋白质乳酸化修饰驱动髓鞘再生的核心机制,为多发性硬化症等脱髓鞘疾病带来了全新的治疗靶点和策略。该研究题为“Oligodendrocyte-encoded lactate dehydrogenase A couples glycolysis to remyelination via protein lactylation”,不仅阐明了成熟少突胶质细胞“为何偏爱糖酵解”这一基础科学问题,也为靶向代谢-表观遗传轴的精准治疗奠定了关键实验基础。

髓鞘损伤是多发性硬化症、阿尔茨海默病等多种神经退行性疾病的共同病理特征,而髓鞘再生失败是导致神经功能障碍难以逆转的根本原因。尽管已知葡萄糖代谢紊乱与髓鞘病变密切相关,但成熟少突胶质细胞究竟依赖何种代谢途径维持髓鞘功能,以及代谢异常如何导致髓鞘修复失败,长期以来悬而未决。
研究团队通过系统的代谢谱分析发现,成熟少突胶质细胞高度依赖由乳酸脱氢酶A(LDHA)驱动的糖酵解代谢,而非传统认为的线粒体氧化磷酸化。在脱髓鞘病变患者及动物模型的病灶中,少突胶质细胞的糖酵解效率显著下降,LDHA表达降低,乳酸生成受阻。通过一系列精细的阶段特异性基因敲除小鼠模型,研究确证了LDHA在少突胶质细胞发育、髓鞘形成和损伤后修复中的核心地位——在少突胶质细胞不同发育阶段敲除LDHA,可分别导致髓鞘发育不良、髓鞘维持障碍及严重的行为学缺陷。
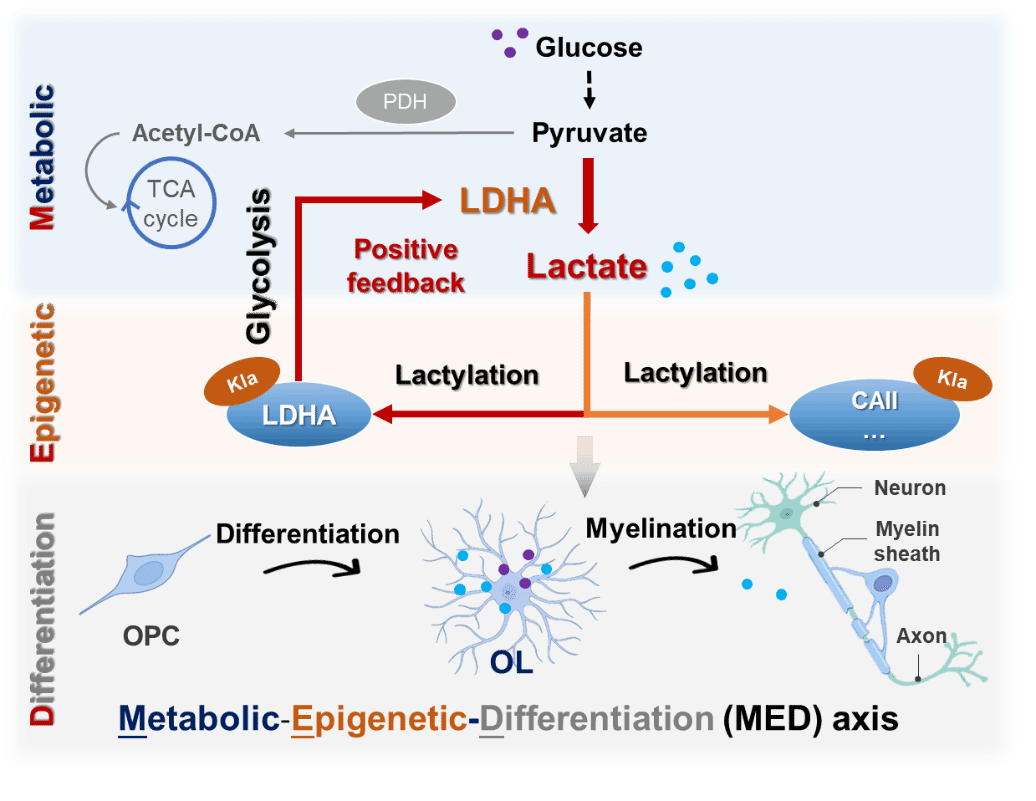
机制上,本研究在髓鞘再生领域确立了乳酸驱动蛋白质乳酸化修饰的全新功能。团队绘制了脱髓鞘病灶的乳酸化修饰全景图谱,并锁定LDHA自身K232位点及碳酸酐酶II(CAII,I/II型少突胶质细胞的特异性标志物)K251位点为功能性修饰靶点,揭示了一个“代谢模式转换-表观遗传修饰-细胞分化增强” 调控网络:糖酵解产生的乳酸通过修饰增强LDHA酶活性,形成“自我加油”式代谢循环,同时激活CAII直接推动少突胶质细胞成熟。该研究颠覆了以往对成熟细胞主要依赖线粒体氧化磷酸化的传统认知,为脱髓鞘疾病的精准治疗开辟了新的酶学治疗靶点。
本研究的通讯作者为公司张媛教授、李星教授和闫亚平教授,博士生包明月、研究生李秀清和博士后孙清清为共同第一作者。研究工作得到了国家自然科学基金等研究经费的支持。
文章链接:https://www.cell.com/neuron/abstract/S0896-6273(26)00137-6

